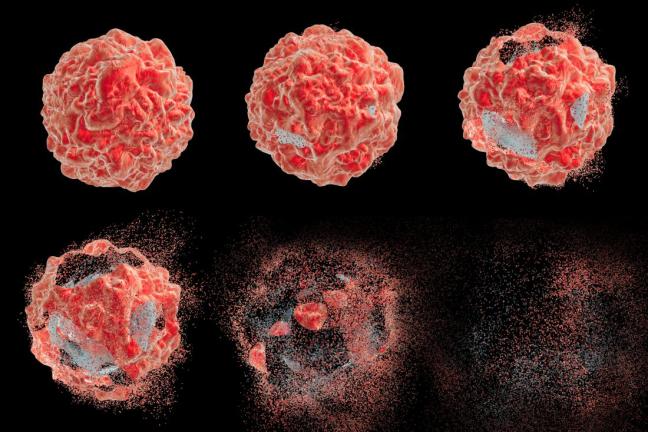
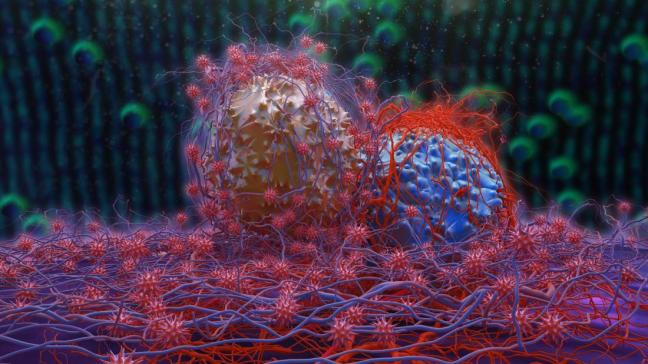
Il cancro è la principale causa di morte in tutto il mondo. Per anni i ricercatori hanno condotto studi meticolosi incentrati su come fermare questa malattia mortale. Quanto siamo vicini alla ricerca di trattamenti più efficaci?

Quanto è arrivata la ricerca sul cancro?
L’Organizzazione Mondiale della Sanità (OMS) nota che, in tutto il mondo, quasi 1 su 6 morti sono a rischio di cancro .
Solo negli Stati Uniti, il National Cancer Institute (NCI) ha stimato 1.688.780 nuovi casi di cancro e 600.920 decessi correlati al cancro nel 2017.
Attualmente, i tipi più comuni di trattamento del cancro sono la chemioterapia , la radioterapia , la chirurgia del tumore e – nel caso del cancro alla prostata e del cancro al seno – la terapia ormonale.
Tuttavia, altri tipi di trattamento stanno iniziando a prendere vapore: terapie che – da sole o in combinazione con altri trattamenti – hanno lo scopo di aiutare a sconfiggere il cancro in modo più efficiente e, idealmente, hanno meno effetti collaterali.
Le innovazioni nel trattamento del cancro mirano ad affrontare una serie di problemi che di solito si trovano ad affrontare operatori sanitari e pazienti, compreso un trattamento aggressivo accompagnato da effetti collaterali indesiderati, recidiva dopo trattamento, chirurgia o entrambi e tumori aggressivi che sono resistenti a trattamenti ampiamente utilizzati.
Di seguito, esaminiamo alcune delle scoperte più recenti della ricerca sul cancro che ci danno una rinnovata speranza che migliori terapie e strategie di prevenzione seguiranno presto le loro mosse.
Promuovere l”arsenale’ del sistema immunitario
Un tipo di terapia che ha attirato molta attenzione di recente è l’ immunoterapia , che mira a rafforzare l’arsenale esistente dei nostri corpi contro corpi estranei e cellule nocive: la risposta del nostro sistema immunitario alla diffusione dei tumori del cancro.
Ma molti tipi di cellule tumorali sono così pericolosi perché hanno modi per “ingannare” il sistema immunitario – o per ignorarli del tutto o per dare loro una ” mano d’aiuto “.
Pertanto, alcuni tipi di cancro aggressivo sono in grado di diffondersi più facilmente e diventare resistenti alla chemioterapia o alla radioterapia.
Tuttavia, grazie agli esperimenti in vitro e in vivo, i ricercatori stanno ora imparando come potrebbero essere in grado di “disattivare” i sistemi di protezione delle cellule tumorali. Uno studio pubblicato lo scorso anno su Nature Immunology ha rilevato che macrofagi, o globuli bianchi, che sono normalmente incaricati di “divorare” detriti cellulari e altri “oggetti” nocivi estranei, non hanno cancellato le cellule tumorali super-aggressive.
Questo perché, nella loro interazione con le cellule tumorali, i macrofagi non leggevano uno ma due segnali intesi a respingere la loro azione di “pulizia”.
Questa conoscenza, tuttavia, ha anche mostrato agli scienziati la via da seguire: bloccando le due vie di segnalazione rilevanti, hanno riabilitato i globuli bianchi per fare il loro lavoro.
Virus terapeutici e innovativi “vaccini”
Un’arma sorprendente nella lotta contro il cancro potrebbe essere un virus terapeutico , come rivelato da una squadra del Regno Unito all’inizio di quest’anno. Nei loro esperimenti, sono riusciti a utilizzare un reovirus per attaccare le cellule tumorali del cervello lasciando al loro posto cellule sane.
“Questa è la prima volta che viene dimostrato che un virus terapeutico è in grado di passare attraverso la barriera cervello-sangue”, ha spiegato gli autori dello studio, che “apre la possibilità [che] questo tipo di immunoterapia possa essere usato per trattare di più persone con tumori cerebrali aggressivi. ”
Un’altra area di miglioramento nell’immunoterapia è “vaccini dendritici”, una strategia in cui le cellule dendritiche (che svolgono un ruolo chiave nella risposta immunitaria del corpo) vengono raccolte dal corpo di una persona, “armato” con antigeni specifici del tumore – che insegnerà loro a “caccia” e distrugge le cellule tumorali rilevanti – e iniettato di nuovo nel corpo per rafforzare il sistema immunitario.
In un nuovo studio , i ricercatori in Svizzera hanno identificato un modo per migliorare l’azione di questi vaccini dendritici creando recettori artificiali in grado di riconoscere e “abdurre” piccole vescicole che sono state collegate alla diffusione di tumori nel corpo.
Attaccando questi recettori artificiali alle cellule dendritiche nei “vaccini”, le cellule terapeutiche sono in grado di riconoscere le cellule tumorali dannose con maggiore accuratezza.
È importante sottolineare che recenti studi hanno dimostrato che l’immunoterapia può funzionare meglio se somministrata in tandem con la chemioterapia, in particolare se i farmaci chemioterapici vengono somministrati per primi e sono seguiti con l’immunoterapia.
Ma questo approccio ha alcune insidie; è difficile controllare gli effetti di questo metodo combinato, quindi a volte i tessuti sani possono essere attaccati insieme ai tumori del cancro.
Tuttavia, gli scienziati di due istituzioni nel North Carolina hanno sviluppato una sostanza che, una volta iniettata nel corpo, diventa gelatinosa: un ” sistema di impalcatura bioresponsivo “. Lo scaffold può contenere contemporaneamente sia la chemioterapia che i farmaci immunoterapici, rilasciandoli sistematicamente nei tumori primari.
Questo metodo consente un migliore controllo di entrambe le terapie, garantendo che i farmaci agiscano sul solo tumore bersaglio.
La rivoluzione delle nanoparticelle
Parlando di strumenti appositamente sviluppati per distribuire farmaci direttamente sul tumore e cacciare i micro-tumori con accuratezza ed efficienza, negli ultimi due anni abbiamo assistito a un “boom” delle nanotecnologie e degli sviluppi delle nanoparticelle per i trattamenti contro il cancro.
Le nanoparticelle potrebbero essere “un punto di svolta” nel trattamento del cancro.
Le nanoparticelle sono particelle microscopiche che hanno raccolto così tanta attenzione nella ricerca clinica, tra gli altri campi, perché ci offrono la possibilità di sviluppare metodi precisi e meno invasivi per affrontare la malattia.
Vitalmente, possono colpire le cellule tumorali o i tumori del cancro senza danneggiare le cellule sane nell’ambiente circostante.
Alcune nanoparticelle sono state create per fornire un trattamento ipertermico molto focalizzato, che è un tipo di terapia che utilizza temperature calde per ridurre i tumori del cancro.
L’anno scorso, scienziati provenienti dalla Cina e dal Regno Unito sono riusciti a inventare un tipo di nanoparticelle ” autoregolatrici ” in grado di esporre i tumori al calore evitando il contatto con tessuti sani.
“Questo potrebbe potenzialmente essere un punto di svolta nel modo in cui trattiamo le persone che hanno il cancro”, ha detto uno dei ricercatori incaricati di questo progetto.
Questi minuscoli veicoli possono anche essere utilizzati per colpire le cellule staminali del cancro , che sono cellule indifferenziate che sono state collegate alla resilienza di alcuni tipi di cancro di fronte a trattamenti tradizionali come la chemioterapia.
Pertanto, le nanoparticelle possono essere “caricate” con farmaci e impostate per “cacciare” le cellule staminali tumorali per prevenire la crescita o la recidiva dei tumori. Gli scienziati hanno sperimentato nanoparticelle riempite di farmaci nel trattamento di vari tipi di cancro, tra cui il cancro al seno e il cancro dell’endometrio .
Non meno importante, i minuscoli veicoli chiamati ” nanosonde ” possono essere utilizzati per rilevare la presenza di micrometastasi, che sono tumori secondari talmente piccoli da non poter essere visti con metodi tradizionali.
Dr. Steven K. Libutti, direttore del Rutgers Cancer Institute del New Jersey a New Brunswick, chiama micrometastasi “tallone di trattamento chirurgico per il tumore d’Achille” e sostiene che nanosonde ‘andare un lungo cammino per risolvere [tali] problemi.’
Strategie di “fame” del tumore
Un altro tipo di strategia che i ricercatori hanno indagato in ritardo è quella dei tumori “affamati” dei nutrienti di cui hanno bisogno per crescere e diffondersi. Questo, gli scienziati sottolineano, potrebbe essere una grazia salvifica nel caso di tumori aggressivi e resilienti che non possono essere sradicati in modo efficace.
Un nuovo metodo per “attaccare” il cancro è quello di “morire di fame” le cellule tumorali fino alla morte.
Tre diversi studi – i cui risultati sono stati tutti pubblicati a gennaio di quest’anno – hanno esaminato i modi per eliminare le scorte nutrizionali del cancro.
Uno di questi studi ha esaminato i modi per fermare la glutammina , un amminoacido presente in natura, dal nutrire le cellule tumorali.
Alcuni tumori, come mammella, polmone e colon, sono noti per utilizzare questo amminoacido per supportare la loro crescita.
Bloccando l’accesso delle cellule tumorali alla glutammina, i ricercatori sono riusciti a massimizzare l’impatto dell’ossidativo stress, un processo che alla fine induce la morte cellulare, su queste cellule.
Alcuni tipi aggressivi di cancro al seno possono essere fermati fermando le cellule da “nutrirsi” di un particolare enzima che li aiuta a produrre l’energia di cui hanno bisogno per prosperare.
Un altro modo per ridurre le cellule cancerogene di energia è bloccando il loro accesso alla vitamina B-2 , come hanno osservato i ricercatori dell’Università di Salford nel Regno Unito.
Come dice un autore dello studio, “Questo è, auspicabilmente, l’inizio di un approccio alternativo per arrestare le cellule staminali del cancro”. Questa strategia potrebbe aiutare le persone che ricevono un trattamento contro il cancro per evitare gli effetti collaterali tossici della chemioterapia.
Trattamenti contro il cancro ed epigenetica
L’epigenetica si riferisce ai cambiamenti causati nei nostri corpi da alterazioni nell’espressione genica, che determinano se alcune caratteristiche appaiono o se determinate “azioni” sono influenzate a livello biologico.
Secondo una ricerca che ha affrontato l’impatto di tali cambiamenti, molti tumori, così come i comportamenti delle cellule tumorali, sono determinati da fattori epigenetici .
“I recenti progressi nel campo dell’epigenetica hanno dimostrato che le cellule tumorali umane ospitano anomalie epigenetiche globali, oltre a numerose alterazioni genetiche”.
“Queste alterazioni genetiche ed epigenetiche interagiscono in tutte le fasi dello sviluppo del cancro, lavorando insieme per promuovere la progressione del cancro”.
Pertanto, è fondamentale per gli specialisti capire quando e dove intervenire e l’espressione di quali geni potrebbero aver bisogno di accendere o spegnere, a seconda del loro ruolo nello sviluppo del cancro.
Uno studio , ad esempio, ha scoperto che il gene responsabile dell’avvento della malattia di Huntington produce un insieme di molecole la cui azione potrebbe effettivamente impedire il verificarsi del cancro.
Ora, la sfida dei ricercatori è incanalare il potenziale terapeutico di questo processo senza innescare la malattia di Huntington. Tuttavia, gli scienziati sono fiduciosi.
“Riteniamo che una terapia per il trattamento del cancro a breve termine per alcune settimane possa essere possibile”, afferma l’autore senior dello studio.
Un altro recente studio è stato in grado di stabilire che i cancri della mammella positivi ai recettori estrogenici che diventano resistenti alla chemioterapia ottengono la loro capacità di recupero attraverso mutazioni genetiche che “conferiscono un vantaggio metastatico al tumore”.
Ma questa conoscenza ha anche dato ai ricercatori la “rottura” di cui avevano bisogno per trovare un trattamento migliore per tali tumori testardi: una terapia combinata che fornisce il farmaco chemioterapico fulvestrant insieme a un inibitore enzimatico sperimentale.
Che cosa significa tutto questo?
La ricerca sul cancro funziona a pieno ritmo, sfruttando tutti i progressi tecnologici che la scienza ha raggiunto negli ultimi anni. Ma cosa significa questo in termini di una cura per il cancro?
Se non ci sarà mai una cura per tutti i tipi di cancro è attualmente una questione di forte dibattito; sebbene gli studi promettenti siano pubblicati e trattati dai media quasi ogni giorno, i tipi di cancro variano enormemente.
Ciò rende molto difficile dire che un approccio che funziona per un tipo sarà adattabile a tutti.
Inoltre, mentre c’è molta ricerca emergente che promette trattamenti più efficaci, la maggior parte di questi progetti sono ancora nelle loro fasi iniziali, avendo condotto esperimenti in vitro e in vivo. Alcuni potenziali trattamenti hanno ancora una lunga strada da percorrere prima degli studi clinici su pazienti umani.
Tuttavia, ciò non significa che dovremmo perdere ogni speranza. Alcuni ricercatori spiegano che questi sforzi dovrebbero renderci ottimisti; mentre noi potremmo non essere nella fase in cui possiamo affermare che il cancro può essere facilmente sradicato, la nostra conoscenza avanzata e strumenti sempre più precisi ci tengono al passo con il gioco e migliorano le nostre probabilità nella lotta contro questa malattia.